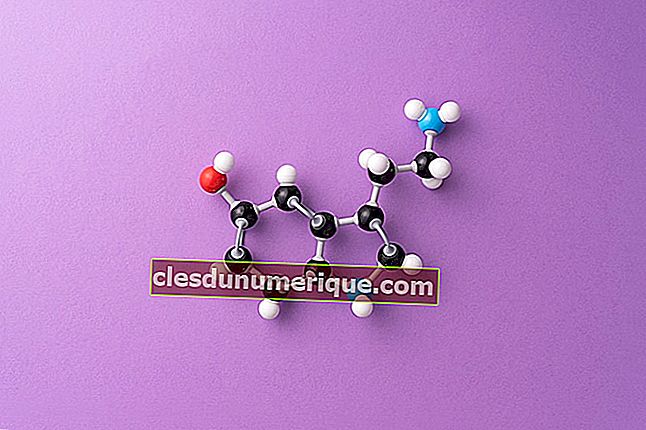
Алканы Алкены Алкины представляют собой группу алифатических углеводородов, состоящую из атома углерода (C) и атомов водорода (H), которые связаны и образуют открытые цепи, которые могут быть разветвленными или нет. Алкановые алкены имеют свои отличия. Давайте рассмотрим различные различия между этими алифатическими углеводородами.
Понимание Алканов Алкенес Алкенес
Одной из уникальности атома углерода является его способность связываться с другими атомами углерода с образованием углеродных цепочек. Самая простая форма углеродной цепи - это углеводороды, которые состоят только из двух элементов: углерода и водорода.
Сами углеводородные соединения имеют соответствующие классификации, основанные на различных факторах. Один из них - алифатические углеводороды, которые в дальнейшем будут разделены на 3 типа связей. Алкановые связи, алкеновые связи и алкиновые связи.
Алканы
Алканы - это простейшие углеродные цепочки с общей формулой:
C n H 2n + 2
Алканы - это насыщенные углеводороды, потому что они имеют одинарные связи. Один из простейших примеров алканов - метан. У метана только один атом углерода связан с четырьмя атомами Н.
Алканы, содержащие 3 или более атомов углерода, могут быть расположены множеством способов, образуя различные структурные изомеры. Самый простой изомер - это когда атом углерода присоединен к одной цепи без каких-либо ответвлений. Этот изомер называется н-изомером (n = «нормальный»).
| Нет. | название | Формула |
| 1 | Метан | CH 4 |
| 2 | Этан | С 2 Н 6 |
| 3 | Пропан | С 3 Н 8 |
| 4 | Бутан | С 4 Н 10 |
| 5 | Пентана | С 5 Н 12 |
| 6 | Гексан | С 6 Н 14 |
| 7 | Гептан | С 7 Н 16 |
| 8 | Октана | С 8 Н 18 |
| 9 | Нонана | C 9 H 20 |
| 10 | Декана | С 10 Н 22 |
| 11 | Октадекана | С 11 Н 36 |
Некоторые из вариантов использования алканов:
- Как топливо.
- Может использоваться как растворитель.
- Как источник водорода.
- Смазочные материалы.
- И другие
Алкенес
Алкены представляют собой ненасыщенные углеводороды и имеют двойные связи (–C = C–). Общая формула, используемая для выражения алкенов:
C 2 H 2n
Другое название Алкенеса - олефин. Простейшей формой алкенов является этен, имеющий формулу C 2 H 4 . Алкены более реактивны по сравнению с алканами. Однако он относительно более стабилен, чем Алкуна.
Алкены также используются в различных областях, таких как:
- Может быть анестетиком при смешивании с содержанием O 2 .
- Созревает плод.
- Сырье из пластмассовой промышленности, синтетический каучук, а также спирт.
Алкуна
Алкины также входят в состав непредельных углеводородных соединений. Однако у алкинов есть одна или несколько тройных связей между атомами углерода. Алкуна имеет общую формулу:
C n H 2n-2
Алкины также называют ацетиленом. Алкины являются более реактивными соединениями по сравнению с алканами и алкенами. Алкены обладают полупроводниковыми свойствами из-за образования полимера под названием полиэтилен, обладающего этими свойствами.
Помимо алканов и алкенов, алкуна также имеет множество применений, таких как:
- Может использоваться в процессе сварки чугуна и стали.
- Может использоваться как освещение.
- Это синтез других соединений.
Вывод
Алканы Алкены Алкины являются частью группы алифатических углеводородов в зависимости от типа связи. Алканы имеют одинарные связи, алкены имеют двойные связи, а алкены имеют тройные связи. Все три имеют множество применений в различных отраслях промышленности.
Это объяснение алифатических углеводородных соединений алканов, алкенов и алкесов. Вы хотите что-нибудь спросить по этому поводу? Если есть, вы можете написать это в колонке комментариев. И не забудьте поделиться этими знаниями с толпой!